|
Tìm kiếm phương trình hóa học
|
| Nhóm Học Miễn Phí Online Facebook | ||||
| Lưu ý: mỗi chất cách nhau 1 khoảng trắng, ví dụ: H2 O2 | ||||
Ca(OH)2 + CO2 = CaCO3 + H2O | Cân Bằng Phương Trình Hóa Học
Ca(OH)2 | canxi hidroxit hoặc tôi vôi | dd + CO2 | Cacbon dioxit | khí = CaCO3 | canxi cacbonat | kt + H2O | nước | lỏng, Điều kiện
Mục Lục
- Cách viết phương trình đã cân bằng
- Thông tin chi tiết về phương trình Ca(OH)2 + CO2 → CaCO3 + H2O
- Điều kiện phản ứng để Ca(OH)2 (canxi hidroxit hoặc tôi vôi) tác dụng CO2 (Cacbon dioxit) là gì ?
- Làm cách nào để Ca(OH)2 (canxi hidroxit hoặc tôi vôi) tác dụng CO2 (Cacbon dioxit)?
- Hiện tượng nhận biết nếu phản ứng xảy ra Ca(OH)2 + CO2 → CaCO3 + H2O là gì ?
- Thông tin nào cần phải lưu ý thêm về phương trình phản ứng Ca(OH)2 + CO2 → CaCO3 + H2O ?
- Giải thích chi tiết về các phân loại của phương trình Ca(OH)2 + CO2 → CaCO3 + H2O
- Chuỗi phương trình hóa học có sử dụng Ca(OH)2 + CO2 → CaCO3 + H2O
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| Ca(OH)2 | + | CO2 | → | CaCO3 | + | H2O | |
| canxi hidroxit hoặc tôi vôi | Cacbon dioxit | canxi cacbonat | nước | ||||
| Carbon dioxide | Calcium carbonate | ||||||
| (dd) | (khí) | (kt) | (lỏng) | ||||
| (trắng) | (không màu) | (trắng) | (không màu) | ||||
| Bazơ | Muối | ||||||
| 74 | 44 | 100 | 18 | ||||
| 1 | 1 | 1 | 1 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Xin hãy kéo xuống dưới để xem và thực hành các câu hỏi trắc nghiệm liên quan
☟☟☟
Thông tin chi tiết về phương trình Ca(OH)2 + CO2 → CaCO3 + H2O
Ca(OH)2 + CO2 → CaCO3 + H2O là Phản ứng trung hoà, Ca(OH)2 (canxi hidroxit hoặc tôi vôi) phản ứng với CO2 (Cacbon dioxit) để tạo ra CaCO3 (canxi cacbonat), H2O (nước) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Ca(OH)2 (canxi hidroxit hoặc tôi vôi) tác dụng CO2 (Cacbon dioxit) là gì ?
Không có
Làm cách nào để Ca(OH)2 (canxi hidroxit hoặc tôi vôi) tác dụng CO2 (Cacbon dioxit) xảy ra phản ứng?
sục khí CO2 qua dung dịch nước vôi trong.
Nếu đang làm bài tập các bạn có thể viết đơn giản là Ca(OH)2 (canxi hidroxit hoặc tôi vôi) tác dụng CO2 (Cacbon dioxit) và tạo ra chất CaCO3 (canxi cacbonat), H2O (nước)
Hiện tượng nhận biết nếu phản ứng xảy ra Ca(OH)2 + CO2 → CaCO3 + H2O là gì ?
Xuất hiện kết tủa trắng Canxi cacbonat (CaCO3) trong dung dịch.
Thông tin nào cần phải lưu ý thêm về phương trình phản ứng Ca(OH)2 + CO2 → CaCO3 + H2O
Dung dịch Ca(OH)2 tác dụng với oxit axit, tạo thành muối và nước.
Phương Trình Điều Chế Từ Ca(OH)2 Ra CaCO3
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Ca(OH)2 (canxi hidroxit hoặc tôi vôi) ra CaCO3 (canxi cacbonat)
Xem tất cả phương trình điều chế từ Ca(OH)2 (canxi hidroxit hoặc tôi vôi) ra CaCO3 (canxi cacbonat)Phương Trình Điều Chế Từ Ca(OH)2 Ra H2O
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Ca(OH)2 (canxi hidroxit hoặc tôi vôi) ra H2O (nước)
Xem tất cả phương trình điều chế từ Ca(OH)2 (canxi hidroxit hoặc tôi vôi) ra H2O (nước)Phương Trình Điều Chế Từ CO2 Ra CaCO3
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ CO2 (Cacbon dioxit) ra CaCO3 (canxi cacbonat)
Xem tất cả phương trình điều chế từ CO2 (Cacbon dioxit) ra CaCO3 (canxi cacbonat)Phương Trình Điều Chế Từ CO2 Ra H2O
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ CO2 (Cacbon dioxit) ra H2O (nước)
Xem tất cả phương trình điều chế từ CO2 (Cacbon dioxit) ra H2O (nước)Giải thích chi tiết về các phân loại của phương trình Ca(OH)2 + CO2 → CaCO3 + H2O
Phản ứng trung hoà là gì ?
Xem tất cả phương trình Phản ứng trung hoà
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình Ca(OH)2 + CO2 → CaCO3 + H2O
Click để xem tất cả câu hỏi có liên quan tới phương trình Ca(OH)2 + CO2 → CaCO3 + H2OCâu 1. Khối lượng của Glucose
Cho glucozơ lên men thành ancol etylic. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hết vào dung dịch Ca(OH)2 dư tạo ra 50 gam kết tủa, biết hiệu suất quá trình lên men đạt 80%. Khối lượng glucozơ cần dùng là
A. 33,70 gam.
B. 56,25 gam.
C. 20,00 gam.
D. 90,00 gam.
Xem đáp án câu 1
Câu 2. Khối lượng tinh bột
Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 75%. Lượng CO2
sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, thu được 60,0 gam kết tủa và dung dịch X. Để
tác dụng tối đa với dung dịch X cần dùng dung dịch chứa 0,2 mol NaOH. Giá trị của m là.
A. 108,0 gam
B. 86,4 gam
C. 75,6 gam
D. 97,2 gam
Xem đáp án câu 2
Câu 3. Khối lượng tinh bột
Lên men m gam tinh bột thành ancol etylic với hiệu suất của cả quá trình là 75%. Lượng CO2 sinh ra được hấp thụ hoàn toàn vào dung dịch Ca(OH)2, thu được 60,0 gam kết tủa và dung dịch X. Để tác dụng tối đa với dung dịch X cần dùng dung dịch chứa 0,2 mol NaOH. Giá trị của m là.
A. 108,0 gam
B. 86,4 gam
C. 75,6 gam
D. 97,2 gam
Xem đáp án câu 3
Câu 4. Tỉ lệ mol
Hấp thụ hoàn toàn 11,2 lít CO2 (đktc) vào dung dịch chứa x mol Ca(OH)2; y mol NaOH và x mol KOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 32,3 gam muối (không có kiềm dư) và 15 gam kết tủa. Bỏ qua sự thủy phân của các ion, tỉ lệ x : y có thể là
A. 2 : 3.
B. 8 : 3.
C. 49 : 33.
D. 4 : 1.
Xem đáp án câu 4
Câu 5. Este
Đốt cháy hoàn toàn 1 lượng hỗn hợp 2 este. Dẫn sản phẩm cháy lần lượt qua bình (1) đựng P2O5 dư và bình (2) đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình (1) tăng 6,21 gam, còn bình (2) thi được 34,5 gam kết tủa. Các este trên thuộc loại este nào sau đây ?
A. Este no, đơn chức, mạch hở
B. Este không no
C. Este thơm
D. Este đa chức
Xem đáp án câu 5
Câu 6. Bài toán khối lượng
Hỗn hợp X gồm metyl fomat, anđehit acrylic và metyl acrylat. Đốt cháy hoàn toàn m gam X rồi hấp thụ hết sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 9 gam kết tủa và khối lượng dung dịch giảm 3,78 gam. Giá trị của m là :
A. 1,95
B. 1,54
C. 1,22
D. 2,02
Xem đáp án câu 6
Câu 7. Bài toán kết tủa
Hấp thụ toàn bộ 0,896 lít CO2 vào 3 lít dd Ca(OH)2 0,01M được:
A. 1 g kết tủa.
B. 2 g kết tủa
C. 3 g kết tủa
D. 4 g kết tủa
Xem đáp án câu 7
Câu 8. Bài toán khối lượng
Lên men hoàn toàn a gam glucozơ, thu được C2H5OH và CO2. Hấp thụ hết CO2 sinh ra vào dung dịch nước vôi trong dư, thu được 15 gam kết tủa. Giá trị của a là:
A. 30,6
B. 27,6
C. 15,3
D. 13,5
Xem đáp án câu 8
Câu 9. Thể tích cần dùng để hấp thụ nước vôi trong
Hỗn hợp X gồm HCHO, CH3COOH, HCOOCH3 và CH3CH(OH)COOH. Đốt cháy hoàn toàn X
cần V lít O2 (đktc), hấp thụ hết sản phẩm cháy vào một lượng dư nước vôi trong thu được 50 gam
kết tủa. Giá trị của V là
A. 8,40.
B. 7,84.
C. 11,2.
D. 16,8.
Xem đáp án câu 9
Câu 10. Dạng toán liên quan tới phản ứng lên men glucozơ
Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với khối lượng dung dịch nước vôi trong ban đầu. Giá trị của m là:
A. 20,0
B. 30,0
C. 13,5
D. 15,0
Xem đáp án câu 10
Câu 11. Dạng toán CO2 tác dụng với dung dịch kiềm
Hấp thụ toàn bộ 0,896 lít CO2 vào 3 lít dd Ca(OH)2 0,01M được:
A. 1g kết tủa
B. 2g kết tủa.
C. 3g kết tủa
D. 4g kết tủa
Xem đáp án câu 11
Câu 12. Bài toán liên quan tới phản ứng lên men glucozơ
Thực hiện lên men ancol từ glucozo (H = 80%) được etanol và khí CO2. Dẫn khí thu được vào dung dịch nước vôi trong dư thu được 40g kết tủa. Lượng glucozo ban đầu là:
A. 45,0 g
B. 36,0 g
C. 28,8 g
D. 43,2 g
Xem đáp án câu 12
Câu 13. Bài toán liên quan tới phản ứng lên men glucozơ
Thực hiện lên men ancol từ glucozo (H = 80%) được etanol và khí CO2. Dẫn khí thu được vào dung dịch nước vôi trong dư thu được 40g kết tủa. Lượng glucozo ban đầu là:
A. 45g
B. 36g
C. 28,8g
D. 43,2g
Xem đáp án câu 13
Câu 14. Bài toán liên quan tới phản ứng lên men glucozơ
Cho m gam glucozơ lên men thành ancol etylic với H = 75%. Toàn bộ khí CO2 sinh ra được hấp thụ hết vào dung dịch Ca(OH)2 lấy dư tạo ra 500g kết tủa. Giá trị của m là: (C=12; H=1, O=16; Ca=40)
A. 720
B. 540
C. 1080
D. 600
Xem đáp án câu 14
Câu 15. Bài toán liên quan tới phản ứng lên men glucozơ
Cho m gam glucozo lên men thành ancol etylic với hiệu suất 60%. Hấp thụ hoàn toàn khí CO2 sinh ra vào nước vôi trong dư thu được 30 gam kết tủa. Giá trị của m là (H=1; O=16; Ca=40; C=12)
A. 45
B. 22,5
C. 11,25
D. 14,4
Xem đáp án câu 15
Câu 16. Bài toán điều chế kim loại bằng phương pháp nhiệt luyện
Cho khí CO đi qua m gam Fe2O3 nung nóng thì thu được 10,68 g chất rắn A và khí B. Cho toàn bộ khí B hấp thụ vào dung dịch Ca(OH)2 dư thì thấy tạo ra 3 gam kết tủa. Giá trị của m là:
A. 11,16g
B. 11,58g
C. 12,0g
D. 12,2g
Xem đáp án câu 16
Câu 17. Bài toán CO2 tác dụng với dung dịch kiềm
Dẫn 8,96 lít CO2 (ở đktc) vào 600 ml dung dịch Ca(OH)2 0,5M. Phản ứng kết thúc thu được m gam kết tủa. Gía trị của m là
A. 40
B. 30
C. 25
D. 20
Xem đáp án câu 17
Câu 18. Bài tập đếm số thí nghiệm thu được kết tủa
Có các thí nghiệm sau (a) Cho kim loại Na vào dung dịch CuSO4; (b) Sục CO2 đến dư vào dung dịch Ca(OH)2; (c) Cho từ từ dung dịch NaOH đến dư vào dung dịch Al2(SO4)3; (d) Cho từ từ dung dịch NaOH đến dư vào dung dịch FeCl3; Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
A. 1
B. 4
C. 3
D. 2
Xem đáp án câu 18
Câu 19. Bài tập đếm số thí nghiệm sinh ra chất khí
Thực hiệ các thí nghiệm sau: (a) Nung NH4NO3 rắn. (b) Đun nóng NaCl tinh thể với dung dịch H2SO4 đặc. (c) Sục khí clo vào dung dịch NaHCO3. (d) Sục khí CO2 vào dung dịch Ca(OH)2 dư. (e) Sục khí SO2 vào dung dịch KMnO4. (g) Cho dung dịch KHSO4 vào dung dịch NaHCO3. (h) Cho PbS vào dung dịch HCl loãng. (i) Cho Na2SO3 vào dung dịch H2SO4 (dư), đun, nóng. Số thí nghiệm sinh ra chất khí là:
A. 4
B. 6
C. 5
D. 2
Xem đáp án câu 19
Câu 20. Tính khối lượng glucozơ được lên men
Lên men hoàn toàn a gam glucozơ, thu được C2H5OH và CO2. Hấp thụ hết CO2 sinh ra vào dung dịch nước vôi trong dư, thu được 15 gam kết tủa. Giá trị của a là:
A. 30,6
B. 27,0
C. 15,3
D. 13,5
Xem đáp án câu 20
Câu 21. Bài toán CO2 tác dụng với dung dịch kiềm
Sục 13,44 lít CO2 (đktc) vào 200 ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M. Sau phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200 ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M thu được m gam kết tủa. Giá trị của m là:
A. 66,98
B. 39,4
C. 47,28
D. 59,1
Xem đáp án câu 21
Câu 22. Tính khối lượng tinh bột dùng trong quá trình lên men
Ancol etylic được điều chế từ tinh bột bằng phương pháp lên men với hiệu suất toàn bộ quá trình là 90%. Hấp thụ toàn bộ lượng CO2 sinh ra khi lên men m gam tinh bột vào nước vôi trong thu được 330 gam kết tủa và dung dịch X. Biết khối lượng X giảm đi so với khối lượng nước vôi trong ban đầu là 132 gam. Giá trị của m là:
A. 324,0.
B. 405,0.
C. 364,5.
D. 328,1.
Xem đáp án câu 22
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiĐánh giá
Chuỗi phương trình hóa học có sử dụng Ca(OH)2 + CO2 → CaCO3 + H2O
Chuỗi phản ứng
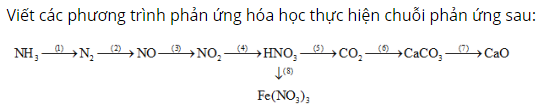
Đốt cháy khí amoniac trong không khí sản phẩm tạo thành có khí thoát ra.
Sau đó, đem khí nito thu được sau phản ứng đốt trong không khí ở nhiệt độ 3000 độ sản phẩm tạo thành khí không màu là NO.
Tiếp đó, đem khí NO để ngoài không khí sau phản ứng khí chuyển thành màu nâu là NO2.
Oxi hóa khí NO2 ở điều kiện thuận lợi sẽ tạo thành axit nitric.
Cho axit HNO3 phản ứng với muối Na2CO3 sản phẩm tạo thành có khí CO2 thoát ra.
Dẫn khí CO2 qua dung dịch nước vôi trong sản phẩm có hiện tượng kết tủa trắng là CaCO3.
Đem muối CaCO3 nhiệt phân ta thu được CaO và khí CO2.
Cuối cùng cho axit nitric hòa tan kim loại sắt sản phẩm thu được là muối Fe(NO3)3 và khí không màu NO thoát ra.
Phương trình liên quan
Có 8 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi phản ứng về kim loại

Nhiệt phân muối canxi cacbonat sản phẩm tạo thành gồm canxi oxit và khí CO2.
Hòa tan CaO trong nước ta thu được nước vôi trong.
Sục khí CO2 qua nước vôi trong sản phẩm tạo thành có hiện tượng kết tủa trắng là CaCO3.
Cho muối canxi cacbonat qua luồng khí CO2 sản phẩm thu được là muối Ca(HCO3)2
Tiếp tục cho muối Ca(HCO3)2 phản ứng với muối Na2CO3 sản phẩm tạo thành gồm 2 muối natri hidrocacbonat và muối canxi cacbonat kết tủa trắng.
Hòa tan muối natri hidrocacbonat trong dung dịch axit HCl sản phẩm tạo thành có khí CO2 thoát ra.
Phương trình liên quan
Có 6 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi phản ứng vô cơ

Đầu tiên nhiệt phân CaCO3 sản phẩm tạo thành CaO và có khí CO2 thoát ra.
Sau đó, cho CaO tác dụng với nước H2O tạo thành Ca(OH)2
Kế tiếp, cho Ca(OH)2 phản ứng với khí CO2 tạo thành CaCO3 kết tủa trắng.
Cho CaCO3 phản ứng với H2O và CO2 sản phẩm tạo thành Ca(HCO3)2
Cuối cùng, nhiệt phân muối Ca(HCO3)2 sản phẩm tạo thành Ca(OH)2 và có khí thoát ra.
Phương trình liên quan
Có 5 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi các phương trình phản ứng của canxi
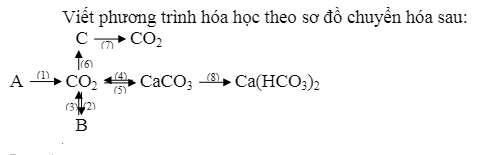
Hòa tan canxi cacbonat trong dung dịch axit HCl sau phản ứng có hiện tượng khí thoát ra là khí CO2.
Tiếp tục cho CO2 phản ứng với cacbon sản phẩm thu được là khí CO.
Sau đó, đem khí CO2 đốt cháy trong không sản phẩm tạo thành là khí CO2.
Tiếp theo nhiệt phân muối canxi cacbonat ta thu được khí CO2.
Sục khí CO2 qua dung dịch nước vôi trong thu được sản phẩm kết tủa là CaCO3.
Tiếp tục đem khí CO2 sục qua dung dịch ntri hidroxit sản phẩm tạo thành là muối natri cacbonat.
Sau đó, đem muối natri cacbonat vừa thu được cho tác dụng với axit HCl sản phẩm thụ được có khí thoát ra là CO2.
Cuối cùng cho khí CO2 có hơi nước phản ứng với CaCO3 sản phẩm tạo thành là canxi hidro cacbonat.
Phương trình liên quan
Có 8 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi các phương trình phản ứng của kim loại canxi
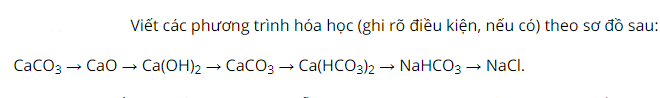
Nhiệt phân muối canxi cacbonat sản phẩm thu được có khí CO2 thoát ra.
Cho canxi oxit tác dụng với nước sản phẩm tạo thành là nước vôi trong.
Sục khí CO2 qua dung dịch nước vôi trong, sau phản ứng có hiện tượng kết tủa trắng là CaCO3.
Cho canxi cacbonat qua luồng khí CO2 có hơi nước sản phẩm tạo thành là canxi hidro cacbonat.
Tiếp tục cho canxi hidro cacbonat tác dụng với natri cacbonat sau phản ứng sản phẩm tạo thành là NaHCO3 và có hiện tượng kết tủa là CaCO3.
Cuối cùng, hòa tan NaHCO3 trong môi trường axit HCl tạo thành muối natri clorua.
Phương trình liên quan
Có 6 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi phương trình hóa học về nito
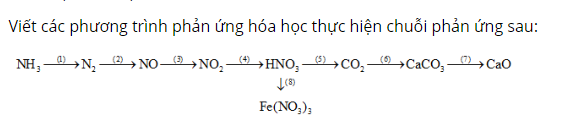
Đốt cháy khí amoniac trong không khí sau phản ứng có hiện tượng khí thoát ra là nito.
Sau đó đem khí nito đốt cháy trong không khí ở nhiệt độ 3000 độ C, sản phẩm tạo thành là khí NO.
Tiếp tục lấy khí NO để ngoài không khí, sau một thời gian có hiện tượng hóa nâu là khí NO2.
Cho khí NO2 tác dụng với oxi có hơi nước tạo thành axit nitric.
Cho axit nitric tác dụng với muối natri cacbonat sau phản ứng có hiện tượng khí thoát ra là khí CO2.
Tiếp tục sục khí CO2 qua dung dịch nước vôi trong sản phẩm có hiện tượng kết tủa trắng là CaCO3.
Nhiệt phân muối CaCO3 thu được CaO và khí CO2.
Sau cùng, cho kim loại sắt hòa tan trong axit nitric sản phẩm tạo thành muối Fe(NO3)3.
Phương trình liên quan
Có 8 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Chuỗi phương trình phản ứng của canxi và hợp chất hữu cơ
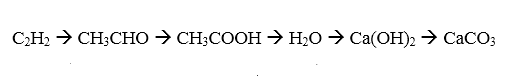
Cho khí axetilen đi qua nước có HgSO4 làm chất xúc tác thu được khí mùi sốc là CH3CHO.
Đốt cháy andehit axetic trong không khí ở nhiệt độ thích hợp và có chất xúc tác thu được axit axetic.
Sau đó cho axit axetic tác dụng với rượu etylic thu được etyl axetat và nước.
Dẫn canxi lội qua nước thu được dung dịch nước vôi trong.
Cuối cùng sục khí CO2 qua dung dịch nước vôi trong thu được sản phẩm có hiện tượng kết tủa trắng là CaCO3.
Phương trình liên quan
Có 5 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Tìm chất A, B, C, D của chuỗi phương trình phản ứng
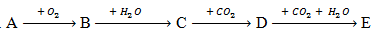
Cho Canxi tác dụng với oxi thu được CaO.
Sau đó, cho canxi oxit lội qua nước thu được Ca(OH)2.
Tiếp tục cho Ca(OH)2 tác dụng với CO2 thu được CaCO3.
Cuối cùng, cho CaCO3 tác dụng với hỗn hợp CO2 và nước thu được Ca(HCO3)2.
Phương trình liên quan
Có 4 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Bài Viết Hóa Học Liên Quan
Bài 26. Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ
Nội dung bài học trình bày cụ thể, tỉ mỉ về Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm, giúp các em học sinh biết được vị trí của kim loại kiềm thổ trong Bảng hệ thống tuần hoàn các nguyên tố hóa học; cấu tạo nguyên tử, tính chất vật lí - hóa học và phương pháp điều chế. Biết được tính chất và ứng dụng của một số hợp chất quan trọng của Kim loại kiềm thổ như Ca(OH) (Canxi hidroxit), CaCO (Canxi cacbonat), CaSO (Canxi sunfat)... Ngoài ra, các em sẽ được tìm hiểu thêm về nước cứng, nguyên tắc và phương pháp làm mềm nước cứng
Bài 5. Luyện tập: Tính chất hóa học của oxit và axit
Oxit bazơ, oxit axit và axit Có những tính chất hoá học nào ? Giữa chúng Có mối quan hệ về tính chất hoá học ra sao ? Vậy giữa oxit và axit liên hệ với nhau như thế nào chúng ta cùng nhau hệ thống lại qua bài hoc sau
Bài 8. Một số bazơ quan trọng
Nội dung bài học nghiên cứu về các vấn đề: Natri hidroxit NaOH và Canxi hidroxitCa(OH) có những tính chất vật lí, tính chất hóa học nào? Những ứng dụng trong đời sống và sản xuất gồm những gì?
Bài 49. Nhận biết một số anion trong dung dịch
Biết phản ứng nhận biết một số anion trong dung dịch
Xác nhận nội dung
Hãy giúp Phương Trình Hóa Học chọn lọc những nội dung tốt bạn nhé!
Bài học liên quan
Các bài học trong sách giáo khoa có sử dụng phương trình hóa học này:
Bài 26. Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ" Bài 5. Luyện tập: Tính chất hóa học của oxit và axit" Bài 8. Một số bazơ quan trọng" Bài 49. Nhận biết một số anion trong dung dịch"Phương trình sản xuất ra Ca(OH)2 (canxi hidroxit hoặc tôi vôi)
(calcium hydroxide)
CaO + H2O → Ca(OH)2 2H2O + CaI2 → Ca(OH)2 + 2HI 2H2O + CaCl2 → Ca(OH)2 + Cl2 + 2H2 Tổng hợp tất cả phương trình điều chế ra Ca(OH)2Phương trình sản xuất ra CO2 (Cacbon dioxit)
(carbon dioxide)
Fe2(CO3)3 + 3H2O → 3CO2 + 2Fe(OH)3 3NH4NO3 + CH2 → 7H2O + 3N2 + CO2 C + O2 → CO2 Tổng hợp tất cả phương trình điều chế ra CO2Phương trình sử dụng CaCO3 (canxi cacbonat) là chất sản phẩm
(calcium carbonate)
CaCO3 + 2HCl → H2O + CO2 + CaCl2 CaCO3 + 2HNO3 → Ca(NO3)2 + H2O + CO2 CaCO3 + H2O + CO2 → Ca(HCO3)2 Tổng hợp tất cả phương trình có CaCO3 tham gia phản ứngPhương trình sử dụng H2O (nước) là chất sản phẩm
(water)
2H2O + 2Na → H2 + 2NaOH CO + H2O + PdCl2 → 2HCl + CO2 + Pd 2H2O + 2KMnO4 + 5SO2 → 2H2SO4 + 2MnSO4 + K2SO4 Tổng hợp tất cả phương trình có H2O tham gia phản ứng















