|
Tìm kiếm phương trình hóa học
|
| Nhóm Học Miễn Phí Online Facebook | ||||
| Lưu ý: mỗi chất cách nhau 1 khoảng trắng, ví dụ: H2 O2 | ||||
2HCl + Zn = H2 + ZnCl2 | Cân Bằng Phương Trình Hóa Học
HCl | axit clohidric | dd + Zn | kẽm | rắn = H2 | hidro | khí + ZnCl2 | Kẽm clorua | dd, Điều kiện
Mục Lục
- Cách viết phương trình đã cân bằng
- Thông tin chi tiết về phương trình 2HCl + Zn → H2 + ZnCl2
- Điều kiện phản ứng để HCl (axit clohidric) tác dụng Zn (kẽm) là gì ?
- Làm cách nào để HCl (axit clohidric) tác dụng Zn (kẽm)?
- Hiện tượng nhận biết nếu phản ứng xảy ra 2HCl + Zn → H2 + ZnCl2 là gì ?
- Thông tin nào cần phải lưu ý thêm về phương trình phản ứng 2HCl + Zn → H2 + ZnCl2 ?
- Giải thích chi tiết về các phân loại của phương trình 2HCl + Zn → H2 + ZnCl2
- Chuỗi phương trình hóa học có sử dụng 2HCl + Zn → H2 + ZnCl2
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| 2HCl | + | Zn | → | H2 | + | ZnCl2 | |
| axit clohidric | kẽm | hidro | Kẽm clorua | ||||
| Hydrogen | |||||||
| (dd) | (rắn) | (khí) | (dd) | ||||
| (không màu) | (ánh kim bạc xám) | (không màu) | (trắng) | ||||
| Axit | Muối | ||||||
| 36 | 65 | 2 | 136 | ||||
| 2 | 1 | 1 | 1 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Xin hãy kéo xuống dưới để xem và thực hành các câu hỏi trắc nghiệm liên quan
☟☟☟
Thông tin chi tiết về phương trình 2HCl + Zn → H2 + ZnCl2
2HCl + Zn → H2 + ZnCl2 là Phản ứng oxi-hoá khửPhản ứng thế, HCl (axit clohidric) phản ứng với Zn (kẽm) để tạo ra H2 (hidro), ZnCl2 (Kẽm clorua) dười điều kiện phản ứng là Không có
Điều kiện phản ứng HCl (axit clohidric) tác dụng Zn (kẽm) là gì ?
Không có
Làm cách nào để HCl (axit clohidric) tác dụng Zn (kẽm) xảy ra phản ứng?
Cho một ít kim loại Kẽm (Zn) vào đáy ống nghiệm, thêm vào ống 1-2 Ml dung dịch axit.
Nếu đang làm bài tập các bạn có thể viết đơn giản là HCl (axit clohidric) tác dụng Zn (kẽm) và tạo ra chất H2 (hidro), ZnCl2 (Kẽm clorua)
Hiện tượng nhận biết nếu phản ứng xảy ra 2HCl + Zn → H2 + ZnCl2 là gì ?
Chất rắn màu xám sẫm Kẽm (Zn) tan dần và xuất hiện bọt khí do khí Hidro (H2) tạo thành.
Thông tin nào cần phải lưu ý thêm về phương trình phản ứng 2HCl + Zn → H2 + ZnCl2
Hiện tại chúng tôi không có thêm bất kỳ thông tin nào thêm về phương trình này. Bạn có thể kéo xuống dưới bạn click vào nút báo lỗi / đóng góp để đưa thêm thông tin
Phương Trình Điều Chế Từ HCl Ra H2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ HCl (axit clohidric) ra H2 (hidro)
Xem tất cả phương trình điều chế từ HCl (axit clohidric) ra H2 (hidro)Phương Trình Điều Chế Từ HCl Ra ZnCl2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ HCl (axit clohidric) ra ZnCl2 (Kẽm clorua)
Xem tất cả phương trình điều chế từ HCl (axit clohidric) ra ZnCl2 (Kẽm clorua)Phương Trình Điều Chế Từ Zn Ra H2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Zn (kẽm) ra H2 (hidro)
Xem tất cả phương trình điều chế từ Zn (kẽm) ra H2 (hidro)Phương Trình Điều Chế Từ Zn Ra ZnCl2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Zn (kẽm) ra ZnCl2 (Kẽm clorua)
Xem tất cả phương trình điều chế từ Zn (kẽm) ra ZnCl2 (Kẽm clorua)Giải thích chi tiết về các phân loại của phương trình 2HCl + Zn → H2 + ZnCl2
Phản ứng oxi-hoá khử là gì ?
Phản ứng oxi hóa khử thường liên quan đến việc chuyển giao điện tử (electron) giữa các đối tượng hóa học. Để hiểu được trọn vẹn phản ứng oxi hoá khử bạn cần hiểu Chất khử: chất khử là chất cho electron, nói cách khác, chất khử sẽ có số oxi hoá tăng sau khi phản ứng xảy ra. Trong định nghĩa của chương trình phổ thông, chất khử cũng được gọi là chất bị oxi hoá. Chất oxi hoá: ngược lại với chất khử, là chất nhận electron. Chất oxi hoá có số oxi hoá tăng sau phản ứng. Chất oxi hoá, trong định nghĩa của chương trình phổ thông còn được gọi là chất bị khừ.
Xem tất cả phương trình Phản ứng oxi-hoá khử
Phản ứng thế là gì ?
Phản ứng trong đó một nguyên tử hoặc nhóm nguyên tử trong phân tử hợp chất hữu cơ bị thay thê bởi một nguyên tử hoặc nhóm nguyên tử khác. Phản ứng thế cũng là một loại phương trình hoá học cực kỳ phổ biến trong chương trình trung học cơ sở và trung học phổ thông.
Xem tất cả phương trình Phản ứng thế
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình 2HCl + Zn → H2 + ZnCl2
Click để xem tất cả câu hỏi có liên quan tới phương trình 2HCl + Zn → H2 + ZnCl2Câu 1. Halogen
Cho các phản ứng sau:
(1). 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O
(2). HCl + NH4HCO3 → NH4Cl + CO2 + H2O
(3). 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O
(4). 2HCl + Zn → ZnCl2 + H2
(5). 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O.
(6). 2HCl + Fe → FeCl2 + H2.
(7). 14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(8). 6HCl + 2Al → 2AlCl3 + 3H2.
(9). 16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Số phản ứng trong đó HCl thể hiện tính oxi hóa, và số phản ứng HCl thể hiện
tính khử là:
A. 2, 5
B. 4, 5
C. 2, 4
D. 3, 5
Xem đáp án câu 1
Câu 2. Bài toán khối lượng
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là
A. 35,7 gam
B. 36,7 gam
C. 53,7gam
D. 63,7 gam
Xem đáp án câu 2
Câu 3. Phản ứng hóa học
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 ?
A. Fe, Ni, Sn
B. Zn, Cu, Mg
C. Hg, Na, Ca
D. Al, Fe, CuO
Xem đáp án câu 3
Câu 4. Chất tác dụng được với HCl và AgNO3
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 ?
A. Fe, Ni, Sn
B. Zn, Cu, Mg
C. Hg, Na, Ca
D. Al, Fe, CuO
Xem đáp án câu 4
Câu 5. Khối lượng muối trong dung dịch
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là
A. 35,7 gam
B. 36,7 gam
C. 53,7gam
D. 63,7 gam
Xem đáp án câu 5
Câu 6. Nhóm oxi lưu huỳnh
Cho các phát biểu sau:
(1). Cho các chất sau: CuO (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), PbS
(6), MgCO3 (7), AgNO3 (8), MnO2 (9), FeS (10). Axit HCl không tác dụng
được với 3 chất.
(2). Axit clohiđric vừa có tính khử vừa có tính oxi hóa .
(3). Dung dịch axit clohiđric có tính axit mạnh.
(4). Cu hòa tan trong dung dịch axit clohiđric khi có mặt O2.
(5). Fe hòa tan trong dung dịch axit clohiđric tạo muối FeCl3.
Số phát biểu sai là:
A. 4
B. 3
C. 2
D. 1
Xem đáp án câu 6
Câu 7. Acid HCl
Cho các phản ứng sau:
(1). 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O
(2). HCl + NH4HCO3 → NH4Cl + CO2 + H2O
(3). 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O
(4). 2HCl + Zn → ZnCl2 + H2
(5). 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O.
(6). 2HCl + Fe → FeCl2 + H2.
(7). 14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(8). 6HCl + 2Al → 2AlCl3 + 3H2.
(9). 16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Số phản ứng trong đó HCl thể hiện tính oxi hóa, và số phản ứng HCl thể hiện
tính khử là:
A. 2, 5
B. 5, 4
C. 4, 2
D. 3, 5
Xem đáp án câu 7
Câu 8. Chất vừa tác dụng được HCl và AgNO3
Các chất vừa tác dụng được với dung dịch HCl vừa tác dụng được với
dung dịch AgNO3 là:
A. CuO, Al, Mg.
B. Zn, Cu, Fe.
C. MgO, Na, Ba.
D. Zn, Ni, Sn.
Xem đáp án câu 8
Câu 9. Các chất tác dụng với HCl và NaOH
Dãy nào sau đây chỉ gồm các kim loại vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH?
A. Al, Zn, Na.
B. Al, Zn, Cr.
C. Ba, Na, Cu.
D. Mg, Zn, Cr.
Xem đáp án câu 9
Câu 10. Lý thuyết về tính chất hóa học của kim loại
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3?
A. Fe, Ni, Sn
B. Zn, Cu, Mg
C. Hg, Na, Ca
D. Al, Fe, CuO
Xem đáp án câu 10
Câu 11. Dạng toán liên quan tới phản ứng kim loại với HCl dư
Cho m gam hỗn hợp kim loại Zn, Cu vào dung dịch HCl (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 4,48 lít H2 (đktc) và 2,0 gam kim loại không tan. Gía trị của m là:
A. 8,50
B. 18,0
C. 15,0
D. 16,0
Xem đáp án câu 11
Câu 12. Xác định các chất tác dụng với dung dịch HCl và AgNO3
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3?
A. Fe, Ni, Sn
B. Zn, Cu, Mg
C. Hg, Na, Ca
D. Al, Fe, CuO
Xem đáp án câu 12
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiĐánh giá
Chuỗi phương trình hóa học có sử dụng 2HCl + Zn → H2 + ZnCl2
Chuỗi phương trình phản ứng hóa học của đồng
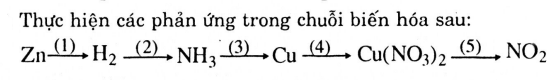
Thả kim loại kẽm trong môi trường axit HCl sau phản ứng thu được khí hidro thoát ra.
Đốt cháy nito với khí hidro tạo thành khí amoniac NH3.
Đốt cháy CuO trong khí NH3 thu được kim loại đồng kết tủa đỏ.
Tiếp theo hòa tan kim loại đồng trong môi trường axit HNO3 loãng thu được muối đồng naitrat.
Nhiệt phân muối đồng nitrat thu được khí NO2 màu nâu.
Phương trình liên quan
Có 5 phương trình phản ứng hóa học liên quan tới chuỗi này.
Hiển thị tối đa 3 phương trình
Vui lòng click "xem chi tiết" để thấy toàn bộ
Bài Viết Hóa Học Liên Quan
Bài 33. Điều chế khí hiđro – Phản ứng thế
Như chúng ta đã biết, những ứng dụng của hidro là không thể bàn cãi. Nhưng khí hidro không có sẵn cho chúng ta sử dụng vào đời sống và sản xuất. Vậy, trong phòng thí nghiệm và trong công nghiệp, khí hidro được điều chế như thế nào? Phản ứng điều chế khí hidro thuộc loại phản ứng gì? Chúng ta sẽ cùng tìm hiểu những vấn đề này trong bài viết sau đây các bạn nhé!
Bài 37. Bài thực hành số 6: Tốc độ phản ứng hóa học
Nội dung bài giảng củng cố lại các kiến thức về các yếu tố ảnh hưởng đến tốc độ phản ứng; rèn luyện kĩ năng quan sát, so sánh các hiện tượng thí nghiệm và giải thích bằng kiến thức đã học.
Bài 26. Phân loại phản ứng trong hóa học vô cơ
Phản ứng hóa học có thể được phân loại theo nhiều cách. Chúng ta hãy làm quen với một vài cách phân loại phản ứng thường gặp trong hóa học vô cơ
Xác nhận nội dung
Hãy giúp Phương Trình Hóa Học chọn lọc những nội dung tốt bạn nhé!
Bài học liên quan
Các bài học trong sách giáo khoa có sử dụng phương trình hóa học này:
Bài 33. Điều chế khí hiđro – Phản ứng thế" Bài 37. Bài thực hành số 6: Tốc độ phản ứng hóa học" Bài 26. Phân loại phản ứng trong hóa học vô cơ"Phương trình sản xuất ra HCl (axit clohidric)
(hydrogen chloride)
CO + H2O + PdCl2 → 2HCl + CO2 + Pd Cl2 + C3H8 → HCl + C3H7Cl CH4 + Cl2 → CH3Cl + HCl Tổng hợp tất cả phương trình điều chế ra HClPhương trình sản xuất ra Zn (kẽm)
(zinc)
2Al + 3Zn(NO3)2 → 3Zn + 2Al(NO3)3 2H2O + 2ZnSO4 → 2H2SO4 + O2 + 2Zn C + ZnO → CO + Zn Tổng hợp tất cả phương trình điều chế ra ZnPhương trình sử dụng H2 (hidro) là chất sản phẩm
(hydrogen)
3H2 + N2 → 2NH3 H2 + S → H2S H2 + CH3[CH2]7CH=CH[CH2]7COOCH3 → CH3[CH2]16COOCH3 Tổng hợp tất cả phương trình có H2 tham gia phản ứngPhương trình sử dụng ZnCl2 (Kẽm clorua) là chất sản phẩm
(zinc chloride)
Mg + ZnCl2 → Zn + MgCl2 2AgNO3 + ZnCl2 → 2AgCl + Zn(NO3)2 4NaOH + ZnCl2 → 2H2O + 2NaCl + Na2ZnO2 Tổng hợp tất cả phương trình có ZnCl2 tham gia phản ứng















