Chuỗi phản ứng về sắt crom
Chuỗi phản ứng về sắt crom
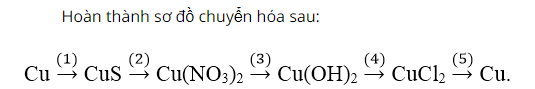
Cho Cu phản ứng với lưu huỳnh tạo thành đồng (II) sunfua. Sau đó, cho CuS tác dụng với axit HNO3 sản phẩm tạo thành có khí NO thoát ra và muối Cu(NO3)2.
Cho muối Cu(NO3)2 tác dụng với dung dịch NaOH sản phẩm thu được kết tủa màu xanh lơ là Cu(OH)2.
Tiếp tục cho Cu(OH)2 tác dụng với dung dịch axit HCl sản phẩm tạo thành có CuCl2.
Cuối cùng điện phân muối CuCl2 thu được khí Cl2 và Cu.
Tóm Tắt Phương Trình Liên Quan
Có 5 phương trình phản ứng hóa học liên quan tới chuỗi này.
Đánh giá
Chi Tiết Phương Trình Liên Quan
Xin lưu ý đây chỉ là phương trình chúng tôi đề nghị, bạn hoàn toàn có thể dùng các phương trình thay thể thỏa điều kiệm của chuỗi
Chi Tiết Phương Trình Số 1
Phương Trình Kết Quả Số #2
Cách viết phương trình đã cân bằng
 |  |  | |||
| Cu | + | S | → | CuS | |
| đồng | sulfua | Đồng sulfat | |||
| Copper | Copper(II) sulfide | ||||
| (rắn) | (rắn) | (kt) | |||
| (đỏ) | (vàng chanh) | (đen) | |||
| Muối | |||||
| 1 | 1 | 1 | Hệ số | ||
| Nguyên - Phân tử khối (g/mol) | |||||
| Số mol | |||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Cu + S → CuS
Cu + S → CuS là Phản ứng oxi-hoá khử, Cu (đồng) phản ứng với S (sulfua) để tạo ra CuS (Đồng sulfat) dười điều kiện phản ứng là Nhiệt độ: ở nhiệt độ phòng Dung môi: CS2 lỏng
Điều kiện phản ứng Cu (đồng) tác dụng S (sulfua) là gì ?
Nhiệt độ: ở nhiệt độ phòng Dung môi: CS2 lỏng
Làm cách nào để Cu (đồng) tác dụng S (sulfua) xảy ra phản ứng?
cho đồng tác dụng với lưu huỳnh
Hiện tượng nhận biết nếu phản ứng xảy ra Cu + S → CuS là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Cu + S → CuS
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình Cu + S → CuS
Click để xem tất cả câu hỏi có liên quan tới phương trình Cu + S → CuSCâu 1. Ozon oxi
Cho các nhận định sau:
(1). Oxi có thể tác dụng với tất cả các kim loại.
(2). Trong công nghiệp oxi được điều chế từ điện phân nước và chưng cất phân
đoạn không khí lỏng.
(3). Khi có ozon trong không khí sẽ làm không khí trong lành.
(4). Ozon được dùng tẩy trắng các loại tinh bột, dầu ăn, khử trùng nước sinh
hoạt, khử mùi, bảo quản hoa quả, chữa sâu răng.
(5). H2O2 được sử dụng làm chất tẩy trắng bột giấy, bột giặt, tơ sợi, lông, len,
vải.Dùng làm chất bảo vệ môi trường.Khử trùng hat giống trong nông nghiệp.
(6). Lưu huỳnh có hai dạng thù hình là đơn tà và tà phương.
(7). Phần lớn S được dùng để sản xuất axit H2SO4.
(8). Các muối CdS, CuS, FeS, Ag2S có màu đen.
(9). SO2 được dùng sản xuất axit sunfuric, tẩy trắng giấy, chống nấm mốc cho
lương thực, thực phẩm.
(10). Ở điều kiện thường SO3 là chất khí tan vô hạn trong nước và H2SO4.
(11). Trong sản xuất axit sunfuric người ta hấp thụ SO3 bằng nước.
Số nhận định đúng là:
A. 7
B. 8
C. 5
D. 6
Xem đáp án câu 1
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 2
Phương Trình Kết Quả Số #3
Cách viết phương trình đã cân bằng
 |  |  |  |  |  | ||||||
| CuS | + | 10HNO3 | → | Cu(NO3)2 | + | 4H2O | + | H2SO4 | + | 8NO2 | |
| Đồng sulfat | axit nitric | Đồng nitrat | nước | axit sulfuric | nitơ dioxit | ||||||
| Copper(II) sulfide | Axit nitric | Copper(II) nitrate | Sulfuric acid; | Nitrogen dioxide | |||||||
| (rắn) | (dd đậm đặc) | (dung dịch) | (lỏng) | (dung dịch) | (khí) | ||||||
| (đen) | (không màu) | (xanh lam) | (không màu) | (không màu) | (nâu đỏ) | ||||||
| Muối | Axit | Muối | Axit | ||||||||
| 1 | 10 | 1 | 4 | 1 | 8 | Hệ số | |||||
| Nguyên - Phân tử khối (g/mol) | |||||||||||
| Số mol | |||||||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình CuS + 10HNO3 → Cu(NO3)2 + 4H2O + H2SO4 + 8NO2
CuS + 10HNO3 → Cu(NO3)2 + 4H2O + H2SO4 + 8NO2 là Phản ứng oxi-hoá khử, CuS (Đồng sulfat) phản ứng với HNO3 (axit nitric) để tạo ra Cu(NO3)2 (Đồng nitrat), H2O (nước), H2SO4 (axit sulfuric), NO2 (nitơ dioxit) dười điều kiện phản ứng là Nhiệt độ: Nhiệt độ.
Điều kiện phản ứng CuS (Đồng sulfat) tác dụng HNO3 (axit nitric) là gì ?
Nhiệt độ: Nhiệt độ.
Làm cách nào để CuS (Đồng sulfat) tác dụng HNO3 (axit nitric) xảy ra phản ứng?
Chúng mình không thông tin về làm thế nào để CuS (Đồng sulfat) phản ứng với HNO3 (axit nitric) và tạo ra chất Cu(NO3)2 (Đồng nitrat) phản ứng với H2O (nước) phản ứng với H2SO4 (axit sulfuric) phản ứng với NO2 (nitơ dioxit).
Bạn có thể kéo xuống dưới và click vào nút báo lỗi để đóng góp thông tin cho chúng mình nhé.Hiện tượng nhận biết nếu phản ứng xảy ra CuS + 10HNO3 → Cu(NO3)2 + 4H2O + H2SO4 + 8NO2 là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình CuS + 10HNO3 → Cu(NO3)2 + 4H2O + H2SO4 + 8NO2
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 3
Phương Trình Kết Quả Số #4
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| Cu(NO3)2 | + | 2NaOH | → | Cu(OH)2 | + | 2NaNO3 | |
| Đồng nitrat | natri hidroxit | Đồng (II) hidroxit | Natri Nitrat | ||||
| Copper(II) nitrate | Sodium hydroxide | Copper(II) hydroxide | Natri nitrat | ||||
| Muối | Bazơ | Muối | Muối | ||||
| 1 | 2 | 1 | 2 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3 là Phản ứng trao đổi, Cu(NO3)2 (Đồng nitrat) phản ứng với NaOH (natri hidroxit) để tạo ra Cu(OH)2 (Đồng (II) hidroxit), NaNO3 (Natri Nitrat) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Cu(NO3)2 (Đồng nitrat) tác dụng NaOH (natri hidroxit) là gì ?
Không có
Làm cách nào để Cu(NO3)2 (Đồng nitrat) tác dụng NaOH (natri hidroxit) xảy ra phản ứng?
Chúng mình không thông tin về làm thế nào để Cu(NO3)2 (Đồng nitrat) phản ứng với NaOH (natri hidroxit) và tạo ra chất Cu(OH)2 (Đồng (II) hidroxit) phản ứng với NaNO3 (Natri Nitrat).
Bạn có thể kéo xuống dưới và click vào nút báo lỗi để đóng góp thông tin cho chúng mình nhé.Hiện tượng nhận biết nếu phản ứng xảy ra Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3 là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
Click để xem tất cả câu hỏi có liên quan tới phương trình Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3Câu 1. Phản ứng tạo đơn chất
Có bao nhiêu phản ứng tạo ra đơn chất trong các phương trình phản ứng sau?
a. C + KNO3 + S →
b.CaO + Cu(NO3)2 + H2O →
c. H2SO4 + KMnO4 + FeSO4 →
d.C + H2O ↔
e. O2 + C12H22O11 →
f. H2 + CH2=CHCH2OH →
h. FeCO3 + HNO3 →
g. Cu(NO3)2 + NaOH →
A. 2
B. 4
C. 5
D. 3
Xem đáp án câu 1
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 4
Phương Trình Kết Quả Số #5
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| Cu(OH)2 | + | 2HCl | → | 2H2O | + | CuCl2 | |
| Đồng (II) hidroxit | axit clohidric | nước | Đồng(II) clorua | ||||
| Copper(II) hydroxide | Copper(II) chloride | ||||||
| (rắn) | (dd) | (lỏng) | (dd) | ||||
| (xanh da trời) | (không màu) | (không màu) | (xanh lá cây) | ||||
| Muối | Axit | Muối | |||||
| 1 | 2 | 2 | 1 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Cu(OH)2 + 2HCl → 2H2O + CuCl2
Cu(OH)2 + 2HCl → 2H2O + CuCl2 là Phản ứng trao đổiPhản ứng trung hoà, Cu(OH)2 (Đồng (II) hidroxit) phản ứng với HCl (axit clohidric) để tạo ra H2O (nước), CuCl2 (Đồng(II) clorua) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Cu(OH)2 (Đồng (II) hidroxit) tác dụng HCl (axit clohidric) là gì ?
Không có
Làm cách nào để Cu(OH)2 (Đồng (II) hidroxit) tác dụng HCl (axit clohidric) xảy ra phản ứng?
cho dd Cu(OH)2 tác dụng với axit HCl
Hiện tượng nhận biết nếu phản ứng xảy ra Cu(OH)2 + 2HCl → 2H2O + CuCl2 là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Cu(OH)2 + 2HCl → 2H2O + CuCl2
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 5
Phương Trình Kết Quả Số #6
Cách viết phương trình đã cân bằng
 |  |  | |||
| CuCl2 | → | Cl2 | + | Cu | |
| Đồng(II) clorua | clo | đồng | |||
| Copper(II) chloride | Chlorine | Copper | |||
| (khí) | (rắn) | ||||
| (vàng lục) | (đỏ) | ||||
| Muối | |||||
| 1 | 1 | 1 | Hệ số | ||
| Nguyên - Phân tử khối (g/mol) | |||||
| Số mol | |||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình CuCl2 → Cl2 + Cu
CuCl2 → Cl2 + Cu là Phương Trình Phản Ứng Hóa Học, CuCl2 (Đồng(II) clorua) để tạo ra Cl2 (clo), Cu (đồng) dười điều kiện phản ứng là Điều kiện khác: Điện phân dung dịch với điện cực trơ
Điều kiện phản ứng CuCl2 (Đồng(II) clorua) là gì ?
Điều kiện khác: Điện phân dung dịch với điện cực trơ
Làm cách nào để CuCl2 (Đồng(II) clorua) xảy ra phản ứng?
Điện phân dung dịch với điện cực trơ CuCl2.
Hiện tượng nhận biết nếu phản ứng xảy ra CuCl2 → Cl2 + Cu là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình CuCl2 → Cl2 + Cu
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiHãy chia sẽ cho bạn bè nếu nếu tài liệu này là hữu ích nhé
Chia sẻ qua facebook
Hoặc chia sẽ link trực tiếp:
http://v1.phuongtrinhhoahoc.com/chuoi-phuong-trinh-hoa-hoc/chuoi-phan-ung-ve-sat-crom-8Xác nhận nội dung
Hãy giúp Phương Trình Hóa Học chọn lọc những nội dung tốt bạn nhé!
















