Chất Hóa Học - H2SO4 - axit sulfuric
sulfuric acid
H2SO4
công thức rút gọn H2O4S
 axit sulfuric
axit sulfuric
 sulfuric acid
sulfuric acid
| Hình ảnh thực tế | Hình công thức cấu tạo | Hình cấu trúc không gian |
Tính chất vật lý
Nguyên tử / Phân tử khối (g/mol) 98.0785
Khối lượng riêng (kg/m3) 1840
Màu sắc Dầu trong suốt, không màu, không mùi
Trạng thái thông thường chất lỏng
Nhiệt độ sôi (°C) 338
Nhiệt độ nóng chảy (°C) 10
Tính chất hóa học
Ứng dụng
Axit sunfuric là một trong hóa chất rất quan trọng, sản lượng axit sunfuric của một quốc gia có thể phản ánh về sức mạnh công nghiệp của quốc gia đó. Phần lớn lượng axit sunfuric (chiếm khoảng 60%) trên thế giới sản xuất ra được tiêu thụ cho phân bón, đặc biệt là superphotphat, amoni photphat và amoni sulfat. Khoảng 20 % axit sunfuric được sử dụng trong công nghiệp hóa chất để sản xuất chất tẩy rửa, nhựa tổng hợp, thuốc nhuộm, dược phẩm, chất xúc tác dầu mỏ, chất diệt côn trùng và chất chống đông, cũng như trong các quy trình khác nhau như axit hóa giếng dầu, khử nhôm, định cỡ giấy và xử lý nước. Khoảng 6% lượng axit sunfuric được sử dụng để sản xuất bột màu như sơn, men, mực in, vải trắng và giấy. Phần còn lại được phân tán vào vô số ứng dụng như sản xuất chất nổ, giấy bóng kính, vải dệt axetat và visco, chất bôi trơn, phi kim loại đen và pin.
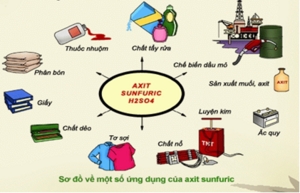
Axit sunfuric là một trong hóa chất rất quan trọng, sản lượng axit sunfuric của một quốc gia có thể phản ánh về sức mạnh công nghiệp của quốc gia đó.
1. Công nghiệp sản xuất hóa chất
Ứng dụng chính của axit sunfuric là trong "phương pháp ướt" để sản xuất axit photphoric , được sử dụng để sản xuất phân bón phốt phát . Trong phương pháp này, đá phốt phát được sử dụng và hơn 100 triệu tấn được xử lý hàng năm. Nguyên liệu thô này được hiển thị bên dưới là fluorapatit , mặc dù thành phần chính xác có thể khác nhau. Chất này được xử lý bằng axit sunfuric 93% để tạo ra canxi sunfat , hydro florua (HF) và axit photphoric .
Amoni sulfat , một loại phân đạm quan trọng, được sản xuất phổ biến nhất như một sản phẩm phụ từ các nhà máy luyện cốc cung cấp cho các nhà máy luyện gang thép. Phản ứng amoniac được tạo ra trong quá trình phân hủy nhiệt của than với axit sunfuric thải cho phép amoniac được kết tinh dưới dạng muối (thường có màu nâu do nhiễm sắt) và được bán vào ngành công nghiệp hóa chất nông nghiệp.
Một ứng dụng quan trọng khác của axit sunfuric là để sản xuất nhôm sunfat , còn được gọi là phèn của nhà sản xuất giấy. Chất này có thể phản ứng với một lượng nhỏ xà phòng trên sợi bột giấy để tạo ra nhôm cacboxylat sền sệt , giúp đông tụ sợi bột giấy thành bề mặt giấy cứng. Nó cũng được sử dụng để sản xuất nhôm hydroxit , được sử dụng tại các nhà máy xử lý nước để lọc tạp chất cũng như cải thiện mùi vị của nước . Nhôm sunfat được tạo ra bằng cách phản ứng bôxit với axit sunfuric.
Axit sulfuric cũng rất quan trọng trong sản xuất dung dịch thuốc nhuộm.
2. Chu trình lưu huỳnh - iot
Các chu kỳ lưu huỳnh i-ốt là một loạt các nhiệt hóa các quá trình có thể sử dụng để sản hydro từ nước . Nó bao gồm ba phản ứng hóa học mà chất phản ứng thực là nước và sản phẩm thực của chúng là hydro và oxy .
Các hợp chất của lưu huỳnh và iốt được thu hồi và tái sử dụng, do đó, quá trình này được coi là một chu trình. Quá trình này là quá trình thu nhiệt và phải xảy ra ở nhiệt độ cao nên phải cung cấp năng lượng dưới dạng nhiệt.
Chu trình lưu huỳnh-iốt đã được đề xuất như một cách để cung cấp hydro cho nền kinh tế dựa trên hydro . Nó là một giải pháp thay thế cho quá trình điện phân và không cần hydrocacbon như các phương pháp cải tạo hơi nước hiện nay . Nhưng lưu ý rằng tất cả năng lượng có sẵn trong hydro được tạo ra được cung cấp bởi nhiệt được sử dụng để tạo ra nó.
Chu trình lưu huỳnh-iốt hiện đang được nghiên cứu như một phương pháp khả thi để thu được hydro, nhưng axit ăn mòn, đậm đặc ở nhiệt độ cao gây ra những nguy cơ an toàn không thể vượt qua nếu quy trình này được xây dựng trên quy mô lớn.
3. Chất tẩy rửa công nghiệp
Axit sulfuric được sử dụng với số lượng lớn bởi các chất sắt và sản xuất thép công nghiệp để loại bỏ quá trình oxy hóa, rỉ sét , và mở rộng quy mô từ tấm cuộn và phôi trước khi bán cho các ô tô và các thiết bị lớn trong ngành.
Axit đã qua sử dụng thường được tái chế bằng cách sử dụng nhà máy tái sinh axit đã qua sử dụng (SAR). Các nhà máy này đốt cháy axit đã qua sử dụng [ cần làm rõ ] bằng khí tự nhiên, khí nhà máy lọc dầu, dầu nhiên liệu hoặc các nguồn nhiên liệu khác. Quá trình đốt cháy này tạo ra khí sulfur dioxide ( SO2) và lưu huỳnh trioxit (SO3) sau đó được sử dụng để sản xuất axit sunfuric "mới". Các nhà máy SAR là sự bổ sung phổ biến cho các nhà máy nấu chảy kim loại, nhà máy lọc dầu và các ngành công nghiệp khác nơi axit sulfuric được tiêu thụ hàng loạt, vì vận hành một nhà máy SAR rẻ hơn nhiều so với chi phí định kỳ của việc xử lý axit đã bỏ ra và mua axit mới.
Dung dịch Piranha thường được sử dụng trong ngành công nghiệp vi điện tử và cả trong phòng thí nghiệm để làm sạch đồ thủy tinh.
4. Chất xúc tác
Axit sulfuric được sử dụng cho nhiều mục đích khác nhau trong ngành công nghiệp hóa chất. Ví dụ, nó là chất xúc tác axit thông thường để chuyển đổi xyclohexanone oxime thành caprolactam , được sử dụng để sản xuất nylon . Nó được sử dụng để sản xuất axit clohydric từ muối thông qua quá trình Mannheim. Axit sunfuric được sử dụng trong tinh chế dầu mỏ , ví dụ như chất xúc tác cho phản ứng của isobutan với isobutylen để tạo ra isooctan , một hợp chất làm tăng chỉ số octan của xăng (xăng). Axit sulfuric cũng thường được sử dụng như một chất khử nước hoặc chất oxy hóa trong các phản ứng công nghiệp, chẳng hạn như sự khử nước của các loại đường khác nhau để tạo thành carbon rắn.
5. Chất điện giải
Axit sunfuric đóng vai trò là chất điện phân trong pin axit - chì
6. Sử dụng trong nước
Axit sulfuric ở nồng độ cao thường là thành phần chính trong chất tẩy rửa cống có tính axit được sử dụng để loại bỏ dầu mỡ , tóc , giấy lụa , v.v. Tương tự như các phiên bản kiềm của chúng , dụng cụ mở ống thoát nước như vậy có thể hòa tan chất béo và protein thông qua quá trình thủy phân . Hơn nữa, vì axit sulfuric đậm đặc có đặc tính khử nước mạnh, nó cũng có thể loại bỏ giấy lụa thông qua quá trình khử nước. Vì axit có thể phản ứng mạnh với nước, các dụng cụ mở ống có tính axit như vậy nên được thêm từ từ vào đường ống để làm sạch.
Đánh giá
Hãy chia sẽ cho bạn bè nếu nếu tài liệu này là hữu ích nhé
Chia sẻ qua facebook
Hoặc chia sẽ link trực tiếp:
http://v1.phuongtrinhhoahoc.com/chat-hoa-hoc-H2SO4-axit+sulfuric-96Các bài học trong SGK
Các bài học trong Sách Giáo Khoa bạn có thể tham khảo thêm
CHƯƠNG 4 OXI – KHÔNG KHÍ
Ở các lớp dưới, các biết gì về nguyên tố oxi, về đơn chất phi kim oxi? Các bạn có nhận xét gì về màu sắc, mùi vị và tính tan trong nước của khí oxi? Oxi có thể tác dụng với các chất khác được không? Nếu được thì mạnh hay yếu? Cụ thể chúng ta sẽ cùng nhau tìm hiểu các vấn đề trên trong bài giảng Tính chất của oxi ngày hôm nay nhé.
Bài 25. Sự oxi hóa – Phản ứng hóa hợp – Ứng dụng của oxi
Tìm hiểu sự oxi hóa là gì và ứng dụng trong đời sống.
Bài 26. Oxit
Các bạn đã biết oxi phản ứng hầu hết các kim loại, và phi kim các. Vậy sản phẩm từ các phản ứng này gọi là gì. Chúng ta cùng tìm hiểu nhé!
Bài 27. Điều chế khí oxi – Phản ứng phân hủy
Khí oxi có rất nhiều trong không khí. Có cách nào tách riêng được khí oxi từ không khí ? Trong phòng thí nghiệm muốn có một lượng nhỏ khí oxi thì làm thế nào ?
Bài 28. Không khí – Sự cháy
Có cách nào để xác định thành phần của không khí ? Không khí có liên quan gì đến sự cháy ? Tại sao khi có gió to thì đám cháy càng dễ bùng cháy to hơn ? Làm thế nào để dập tắt được đám cháy và tốt hơn là để đám cháy không xảy ra ?
Các câu hỏi có liên quan tới chất hóa học H2SO4 (axit sulfuric)
Dưới đây là các câu hỏi về liệu H2SO4 có thể tác dụng với chất nào khác không. Bạn có thể
H2SO4 có tác dụng với I2 không? H2SO4 có tác dụng với K không? H2SO4 có tác dụng với K2CO3 không? H2SO4 có tác dụng với K2Cr2O7 không? H2SO4 có tác dụng với K2O không? H2SO4 có tác dụng với K2S không? H2SO4 có tác dụng với K2S2O8 không? H2SO4 có tác dụng với K3PO4 không? H2SO4 có tác dụng với KBr không? H2SO4 có tác dụng với KCl không? H2SO4 có tác dụng với KClO3 không? H2SO4 có tác dụng với KI không? H2SO4 có tác dụng với KMnO4 không? H2SO4 có tác dụng với KNO2 không? H2SO4 có tác dụng với KNO3 không? H2SO4 có tác dụng với KOH không? H2SO4 có tác dụng với Li không? H2SO4 có tác dụng với Mg không? H2SO4 có tác dụng với Mg(NO3)2 không? H2SO4 có tác dụng với Mg(OH)2 không? H2SO4 có tác dụng với MgCO3 không? H2SO4 có tác dụng với Mn không? H2SO4 có tác dụng với MnO2 không? H2SO4 có tác dụng với MnSO4 không? H2SO4 có tác dụng với N2 không? H2SO4 có tác dụng với N2O5 không? H2SO4 có tác dụng với Na không? H2SO4 có tác dụng với Na2CO3 không? H2SO4 có tác dụng với Na2HPO4 không? H2SO4 có tác dụng với Na2O không? H2SO4 có tác dụng với Na2S không? H2SO4 có tác dụng với Na2S2O3 không? H2SO4 có tác dụng với Na2SiO3 không? H2SO4 có tác dụng với Na2SO3 không? H2SO4 có tác dụng với Na2SO4 không? H2SO4 có tác dụng với Na3PO4 không? H2SO4 có tác dụng với NaCH3COO không? H2SO4 có tác dụng với NaCl không? H2SO4 có tác dụng với NaClO không? H2SO4 có tác dụng với NaHCO3 không? H2SO4 có tác dụng với NaI không? H2SO4 có tác dụng với NaNO2 không? H2SO4 có tác dụng với NaNO3 không? H2SO4 có tác dụng với NaOH không? H2SO4 có tác dụng với NH3 không? H2SO4 có tác dụng với NH4Cl không? H2SO4 có tác dụng với NH4NO2 không? H2SO4 có tác dụng với NH4NO3 không? H2SO4 có tác dụng với NO không? H2SO4 có tác dụng với NO2 không? H2SO4 có tác dụng với O2 không? H2SO4 có tác dụng với O3 không? H2SO4 có tác dụng với P không? H2SO4 có tác dụng với P2O5 không? H2SO4 có tác dụng với Pb(NO3)2 không? H2SO4 có tác dụng với Pb(OH)2 không? H2SO4 có tác dụng với PH3 không? H2SO4 có tác dụng với PI3 không? H2SO4 có tác dụng với Pt không? H2SO4 có tác dụng với S không? H2SO4 có tác dụng với Si không? H2SO4 có tác dụng với SiO2 không? H2SO4 có tác dụng với Sn(OH)2 không? H2SO4 có tác dụng với SO2 không? H2SO4 có tác dụng với SO3 không? H2SO4 có tác dụng với Zn không? H2SO4 có tác dụng với Zn3P2 không? H2SO4 có tác dụng với ZnO không? H2SO4 có tác dụng với ZnS không? H2SO4 có tác dụng với ZnSO4 không? H2SO4 có tác dụng với ZnCl2 không? H2SO4 có tác dụng với N2O4 không? H2SO4 có tác dụng với N2O không? H2SO4 có tác dụng với HNO2 không? H2SO4 có tác dụng với NiO không? H2SO4 có tác dụng với CrO3 không? H2SO4 có tác dụng với Mn2O7 không? H2SO4 có tác dụng với Ni(OH)3 không? H2SO4 có tác dụng với Li2O không? H2SO4 có tác dụng với Ba không? H2SO4 có tác dụng với TiO2 không? H2SO4 có tác dụng với TiCl4 không? H2SO4 có tác dụng với Be(OH)2 không? H2SO4 có tác dụng với Mg(HCO3)2 không? H2SO4 có tác dụng với NH4OH không? H2SO4 có tác dụng với NaAlO2 không? H2SO4 có tác dụng với PbO không? H2SO4 có tác dụng với FeSO4 không? H2SO4 có tác dụng với MnO không? H2SO4 có tác dụng với MgCl2 không? H2SO4 có tác dụng với MgO không? H2SO4 có tác dụng với BeCl2 không? H2SO4 có tác dụng với Be không? H2SO4 có tác dụng với BeO không? H2SO4 có tác dụng với Be(NO3)2 không? H2SO4 có tác dụng với H2ZnO2 không? H2SO4 có tác dụng với HAlO2.H2O không? H2SO4 có tác dụng với Cu2O không? H2SO4 có tác dụng với Zn(OH)2 không? H2SO4 có tác dụng với PdCl2 không?Xác nhận nội dung
Hãy giúp Phương Trình Hóa Học chọn lọc những nội dung tốt bạn nhé!
Phương trình có H2SO4 (axit sulfuric) là chất tham gia
sulfuric acid
H2SO4 + Na2SO3 → H2O + Na2SO4 + SO2 10FeO + 18H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 18H2O + 2MnSO4 + K2SO4 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 Xem tất cả phương trình sử dụng H2SO4Phương trình có H2SO4 (axit sulfuric) là chất sản phẩm
sulfuric acid
2H2O + 2KMnO4 + 5SO2 → 2H2SO4 + 2MnSO4 + K2SO4 24HNO3 + FeCuS2 → Cu(NO3)2 + 10H2O + 2H2SO4 + 18NO2 + Fe(NO3)3 Fe2(SO4)3 + 3H2O → 2Fe + 3H2SO4 + 3/2O2 Xem tất cả phương trình tạo ra H2SO4
















