Chuỗi phản ứng halogen của iot và brom
Chuỗi các phương trình phản ứng của các halogen thường gặp trong sách giáo khoa Hóa học lớp 10.
Chuỗi phản ứng halogen của iot và brom
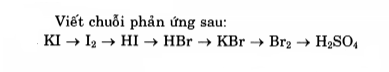
Cho KI tác dụng với clo tạo thành có hiện tượng kết tủa tím là iot.
Tiếp tục đốt cháy iot với khí hidro tạo thành HI.
Dẫn HI qua nước brom tạo thành HBr.
Tiếp tục cho HBr hòa tan trong dung dịch KOH tạo thành KBr.
Sau đó điện phân dung dịch KBr có màng ngăn thu được khí brom.
Cuối cùng, sục nước brom qua khí SO2 tạo thành axit sunfuric.
Tóm Tắt Phương Trình Liên Quan
Có 4 phương trình phản ứng hóa học liên quan tới chuỗi này.
Đánh giá
Chi Tiết Phương Trình Liên Quan
Xin lưu ý đây chỉ là phương trình chúng tôi đề nghị, bạn hoàn toàn có thể dùng các phương trình thay thể thỏa điều kiệm của chuỗi
Chi Tiết Phương Trình Số 1
Phương Trình Kết Quả Số #2
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| Cl2 | + | 2KI | → | I2 | + | 2KCl | |
| clo | kali iodua | Iot | kali clorua | ||||
| Chlorine | Kali clorua | ||||||
| (khí) | (dd) | (rắn) | (rắn) | ||||
| (vàng lục) | (đen tím) | ||||||
| Muối | Muối | ||||||
| 1 | 2 | 1 | 2 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Cl2 + 2KI → I2 + 2KCl
Cl2 + 2KI → I2 + 2KCl là Phản ứng oxi-hoá khử, Cl2 (clo) phản ứng với KI (kali iodua) để tạo ra I2 (Iot), KCl (kali clorua) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Cl2 (clo) tác dụng KI (kali iodua) là gì ?
Không có
Làm cách nào để Cl2 (clo) tác dụng KI (kali iodua) xảy ra phản ứng?
cho clo tác dụng với KI
Hiện tượng nhận biết nếu phản ứng xảy ra Cl2 + 2KI → I2 + 2KCl là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Cl2 + 2KI → I2 + 2KCl
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình Cl2 + 2KI → I2 + 2KCl
Click để xem tất cả câu hỏi có liên quan tới phương trình Cl2 + 2KI → I2 + 2KClCâu 1. Chất làm hồ tinh bôt hóa xanh
Có dung dịch X gồm (KI và một ít hồ tinh bột). Cho lần lượt từng chất
sau: O3, Cl2, Br2, FeCl3, AgNO3 tác dụng với dung dịch X. Số chất làm
dung dịch X chuyển sang màu xanh là:
A. 3 chất.
B. 4 chất.
C. 2 chất.
D. 5 chất.
Xem đáp án câu 1
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 2
Phương Trình Kết Quả Số #3
Cách viết phương trình đã cân bằng
 |  |  | |||
| H2 | + | I2 | ↔ | 2HI | |
| hidro | Iot | axit iodic | |||
| Hydrogen | Hydrogen iodide | ||||
| (khí) | (rắn) | (khí) | |||
| (không màu) | (đen tím) | (không màu) | |||
| Axit | |||||
| 1 | 1 | 2 | Hệ số | ||
| Nguyên - Phân tử khối (g/mol) | |||||
| Số mol | |||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình H2 + I2 → 2HI
H2 + I2 → 2HI là Phản ứng hoá hợpPhản ứng oxi-hoá khử, H2 (hidro) phản ứng với I2 (Iot) để tạo ra HI (axit iodic) dười điều kiện phản ứng là Nhiệt độ: 350 - 500°C Xúc tác: Pt
Điều kiện phản ứng H2 (hidro) tác dụng I2 (Iot) là gì ?
Nhiệt độ: 350 - 500°C Xúc tác: Pt
Làm cách nào để H2 (hidro) tác dụng I2 (Iot) xảy ra phản ứng?
hidro tác dụng với I2
Hiện tượng nhận biết nếu phản ứng xảy ra H2 + I2 → 2HI là gì ?
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm HI (axit iodic) (trạng thái: khí) (màu sắc: không màu), được sinh ra
Hoặc bạn phải quan sát chất tham gia H2 (hidro) (trạng thái: khí) (màu sắc: không màu), I2 (Iot) (trạng thái: rắn) (màu sắc: đen tím), biến mất.
Giải thích chi tiết về các phân loại của phương trình H2 + I2 → 2HI
Câu hỏi bài tập trắc nghiệm và tư luận có sử dụng phương trình H2 + I2 → 2HI
Click để xem tất cả câu hỏi có liên quan tới phương trình H2 + I2 → 2HICâu 1. Cân bằng hóa học
Cho các cân bằng:
1) H2 + I2(rắn) ←→ 2HI
2) N2 + 3H2 ←→ 2NH3
3) H2 + Cl2 ←→ 2HCl
4) 2SO2 (k) + O2 (k) ←→ 2SO3
5) SO2 + Cl2 ←→ SO2Cl2
Khi tăng áp suất chung của cả hệ số cân bằng chuyển dịch theo chiều thuận và
chiều nghịch lần lượt là:
A. 3 và 2
B. 3 và 1
C. 2 và 4
D. 2 và 5
Xem đáp án câu 1
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 3
Phương Trình Kết Quả Số #4
Cách viết phương trình đã cân bằng
 |  |  |  | ||||
| Br2 | + | 2HI | → | I2 | + | 2HBr | |
| brom | axit iodic | Iot | Hidro bromua | ||||
| Bromine | Hydrogen iodide | Axit bromhydric | |||||
| (lỏng) | (dd) | (rắn) | (khí) | ||||
| (nâu đỏ) | (đen tím) | (không màu) | |||||
| Axit | Axit | ||||||
| 1 | 2 | 1 | 2 | Hệ số | |||
| Nguyên - Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Br2 + 2HI → I2 + 2HBr
Br2 + 2HI → I2 + 2HBr là Phản ứng oxi-hoá khử, Br2 (brom) phản ứng với HI (axit iodic) để tạo ra I2 (Iot), HBr (Hidro bromua) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Br2 (brom) tác dụng HI (axit iodic) là gì ?
Không có
Làm cách nào để Br2 (brom) tác dụng HI (axit iodic) xảy ra phản ứng?
cho brom tác dụng với HI
Hiện tượng nhận biết nếu phản ứng xảy ra Br2 + 2HI → I2 + 2HBr là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Br2 + 2HI → I2 + 2HBr
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiChi Tiết Phương Trình Số 6
Phương Trình Kết Quả Số #5
Cách viết phương trình đã cân bằng
 |  |  |  |  | |||||
| Br2 | + | H2O | + | SO2 | → | H2SO4 | + | 2HBr | |
| brom | nước | lưu hùynh dioxit | axit sulfuric | Hidro bromua | |||||
| Bromine | Sulfur đioxit | Sulfuric acid; | Axit bromhydric | ||||||
| (lỏng) | (lỏng) | (khí) | (lỏng) | (lỏng) | |||||
| (nâu đỏ) | (không màu) | (không màu) | (không màu) | (không màu) | |||||
| Axit | Axit | ||||||||
| 1 | 1 | 1 | 1 | 2 | Hệ số | ||||
| Nguyên - Phân tử khối (g/mol) | |||||||||
| Số mol | |||||||||
| Khối lượng (g) |
Thông tin chi tiết về phương trình Br2 + H2O + SO2 → H2SO4 + 2HBr
Br2 + H2O + SO2 → H2SO4 + 2HBr là Phản ứng oxi-hoá khử, Br2 (brom) phản ứng với H2O (nước) phản ứng với SO2 (lưu hùynh dioxit) để tạo ra H2SO4 (axit sulfuric), HBr (Hidro bromua) dười điều kiện phản ứng là Không có
Điều kiện phản ứng Br2 (brom) tác dụng H2O (nước) tác dụng SO2 (lưu hùynh dioxit) là gì ?
Không có
Làm cách nào để Br2 (brom) tác dụng H2O (nước) tác dụng SO2 (lưu hùynh dioxit) xảy ra phản ứng?
Sục khí SO2 vào dung dịch Brom
Hiện tượng nhận biết nếu phản ứng xảy ra Br2 + H2O + SO2 → H2SO4 + 2HBr là gì ?
Click để xem thông tin thêmGiải thích chi tiết về các phân loại của phương trình Br2 + H2O + SO2 → H2SO4 + 2HBr
Báo lỗi cân bằng
Nếu bạn nhận ra phương trình này chưa được cân bằng chính xác. Hãy click vào nút bên dưới để thông báo cho chúng mình biết nhé
Click vào đây để báo lỗiHãy chia sẽ cho bạn bè nếu nếu tài liệu này là hữu ích nhé
Chia sẻ qua facebook
Hoặc chia sẽ link trực tiếp:
http://v1.phuongtrinhhoahoc.com/chuoi-phuong-trinh-hoa-hoc/chuoi-phan-ung-halogen-cua-iot-va-brom-55Xác nhận nội dung
Hãy giúp Phương Trình Hóa Học chọn lọc những nội dung tốt bạn nhé!
















